La farmacéutica Merck solicitó este lunes a los reguladores estadounidenses que autoricen su píldora contra el Covid-19, la cual reduce en un 50% el riesgo de hospitalización o muerte en pacientes con esta enfermedad, indicó la compañía.
Ahora bien, si la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) autoriza la píldora, dicha decisión que podría llegar en unas cuantas semanas y sería la primera que pueda demostrar que puede tratar el coronavirus. También los demás tratamientos respaldados por la FDA requieren una vía intravenosa o una inyección.
 Foto: CNN en Español
Foto: CNN en Español¿Cómo ayudaría la píldora contra el Covid-19?
Se trata de una píldora antiviral que las personas podrán tomar en casa para reducir síntomas y acelerar la recuperación. Además, que frenaría la carga de trabajo en hospitales y ayudaría a frenar brotes en los países más pobres con sistemas sanitarios débiles.
La FDA indagará sobre los datos de seguridad que proporciona la empresa y la eficacia del medicamento, el molnupiravir, antes de tomar dicha decisión.
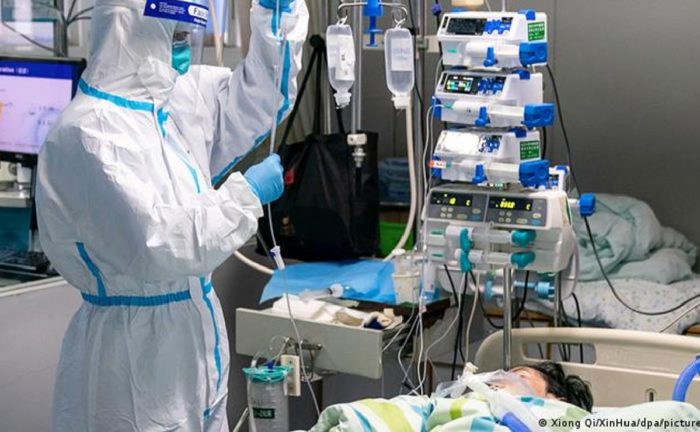 Foto: DW
Foto: DWLos laboratorios, Merck y Ridgeback Bitherapeutic solicitaron a la agencia que otorgara el uso de emergencia en adultos con Covid-19 en estado leve o moderado que corren riesgo de agravarse.
A principios de este mes la farmacéutica informó los beneficios de la píldora en pacientes con síntomas tempranos de Covid-19. Sin embargo, los resultados fueron contundentes que expertos médicos supervisaron el ensayo recomendaron suspenderlo antes.
 Foto: France 24
Foto: France 24Efectos secundarios similares en pacientes que recibieron el fármaco y otro grupo que recibieron una píldora placebo. No obstante, la farmacéutica Merck no ha detallado públicamente los tipos de problemas registrados, que serán parte clave para la indagación de la FDA.
Por otro lado, las autoridades estadounidenses promueven la vacunación como la mejor manera de protegerse ante el virus. Pero alrededor de 68 millones de estadounidenses no están dispuestos a vacunarse, los fármacos son fundamentales para prevenir futuras oleadas de infección.
 Foto: France 24
Foto: France 24La farmacéutica ha firmado acuerdos de licencia con fabricantes de medicamentos genéricos de la India para producir versiones de bajo costo para los países más con sistema de salud débil.
También empresas, como Pfizer y Roche, están estudiando fármacos semejantes y se espera una respuesta durante los próximos meses. Mientras que AstraZeneca espera la autorización de la FDA.